Witness (testificación electrónica)
La testificación electrónica es un sistema de identificación que permite diferenciar las muestras en el laboratorio con un código personal único, ofreciendo el máximo nivel de trazabilidad en el manejo de muestras.
Somos el primer centro en el Perú y el tercero en Latinoamérica en contar con el sistema RI Witness, un sistema de radiofrecuencia (RFID) que utiliza chips de identificación fijados a cada objeto que contengan las muestras. El objetivo es evitar al máximo cualquier posible confusión que pudiese ocurrir durante los procedimientos de reproducción asistida.
RI Witness utiliza identificación por RFID para detectar y controlar toda la actividad en el laboratorio de FIV. El sistema ayuda a mitigar el riesgo de error humano cada vez que las muestras se mueven de un plato o tubo a otro, y protege cada paso del ciclo de FIV.
En todo el laboratorio, los lectores de RI Witness se encuentran en todos los lugares en los que se realiza el trabajo de manera crítica y donde se manejan las muestras (gametos y embriones). Las placas de embriología calentadas o no calentadas con lectores RFID incorporados se pueden así manejar con tranquilidad. Estos lectores están activos todo el día, todos los días, por lo que no se puede pasar por alto un control.
Por lo tanto, disponer de RI Witness ayuda a prevenir posibles errores y gestiona la actividad en los laboratorios de FIV. El uso de RI Witness significa que los miembros del personal del laboratorio de las clínicas de fertilidad y los pacientes de FIV disfrutan de una tranquilidad adicional, así como de beneficios adicionales en la eficiencia de los tratamientos.


Cultivo extendido (hasta blastocisto)
Para aumentar las probabilidades de éxito de las técnicas de reproducción asistida es de vital importancia mantener las condiciones de cultivo en el laboratorio y seleccionar los mejores embriones desde el inicio para transferir.
Los ovocitos fecundados continúan su crecimiento en condiciones específicas en las incubadoras por 5 o 6 días, evitando la mayor cantidad de perturbaciones hasta su transferencia al útero materno. En el día 5 del desarrollo empieza a formarse una cavidad dentro del embrión y se produce la diferenciación celular. A esta nueva morfología del embrión se le denomina blastocisto.
En condiciones naturales este proceso de desarrollo ocurre durante el camino del embrión hacia el útero a través de la trompa de Falopio. Cuando el blastocisto llega a la cavidad uterina, está listo para iniciar su implantación en el endometrio materno. Por ello, es muy importante que durante el tiempo que los embriones están en las incubadoras se les proporcione un ambiente controlado y que se asemeje mucho al ambiente materno.
Hasta hace algunos años, la tecnología no permitía cultivar los embriones más allá del día 3 de desarrollo, con los avances tecnológicos (mejores incubadoras, y medios de cultivo y mayor conocimiento de la biología del desarrollo embrionario) ahora se puede extender el cultivo embrionario hasta la etapa de blastocisto (día 5 – 6 del desarrollo). Los beneficios son permitir una mejor selección embrionaria, al mismo tiempo que se imita el proceso natural que ocurre en las trompas de Falopio, todo lo cual contribuye a aumentar significativamente las posibilidades de embarazo.
Vitrificación
La vitrificación es una técnica de criopreservación ampliamente utilizada que se basa en la congelación ultrarrápida de las células evitando la formación de cristales de hielo y daño de las estructuras internas. Con la vitrificación podemos congelar tanto ovocitos (óvulos) como embriones.
Luego de realizado el proceso de vitrificación, los ovocitos y embriones son almacenados en nuestros tanques de nitrógeno líquido a -196°C hasta el momento en el que desee utilizarlos. Aquí pueden estar conservados por tiempo indefinido y de forma segura, manteniendo (tanto ovocitos como embriones) las mismas características que tenían al momento de la congelación.
La vitrificación ha mostrado aumentar la sobrevivencia de los ovocitos en comparación con la técnica más antigua de congelación lenta, además no altera las tasas de éxito de los tratamientos de reproducción asistida al mantener sus características iniciales, siendo similares a los resultados obtenidos con ovocitos frescos. La congelación de ovocitos ha permitido entre otras ventajas optimizar los tratamientos de preservación de la fertilidad en la mujer, así como también aumentar las tasas de éxito en los casos de ovodonación.

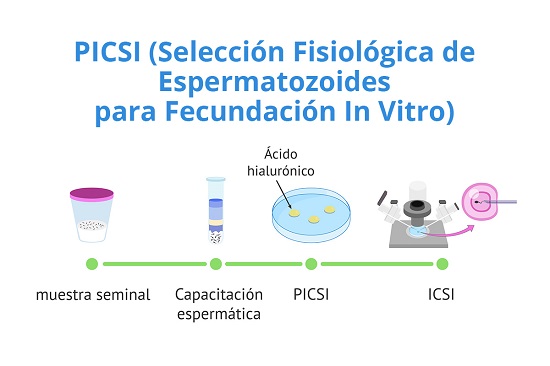



SMART ICSI (PICSI + SLICSI)
Somos el primer centro en el Perú en contar con el sistema SLICSI (del inglés Splindle Location ICSI). El SLICSI es una técnica que utiliza la microscopia de luz polarizada permitiendo la localización del huso meiótico para así valorar el nivel de maduración de los ovocitos (óvulos) previo a la ICSI.
Diversos estudios científicos han demostrado la utilidad de la microscopía de luz polarizada encontrándose: mejor ajuste del momento en el cual debe realizarse la ICSI al evaluar el estado de maduración del ovocito, mejores tasas de fecundación, de formación de blastocisto y de embarazo en general. Una ventaja adicional de SLICSI es que se evita un posible daño mecánico al ovocito durante el proceso de ICSI al visualizarse correctamente al huso.
El SMART ICSI es una combinación perfecta de la técnica de PICSI (ICSI con selección fisiológica de espermatozoides) y SLICSI. De esta manera, a la mejor selección de espermatozoides por PICSI le sumamos las ventajas de una correcta elección y visualización de los ovocitos gracias a SLICSI. Con esta combinación innovadora utilizada en el laboratorio de embriología de CERAS, nuestro objetivo es lograr las más altas posibilidades de éxito en los tratamientos de reproducción asistida de alta complejidad.
Biopsia embrionaria
El procedimiento de biopsia embrionaria es una técnica por el cual se extrae una pequeña cantidad de células del embrión en desarrollo. Estas células extraídas al ser procesadas en el laboratorio de genética permiten analizar su composición genética y/o cromosómica con el fin de buscar alguna alteración.
En nuestro centro la biopsia embrionaria se realiza en embriones en etapa de blastocisto, es una técnica que requiere de gran precisión y experiencia por parte del embriólogo. Básicamente, la técnica consiste en la extracción de una pequeña cantidad de células de la capa celular externa del blastocisto denominada trofoectodermo, con la ayuda de un láser. Las células del trofoectodermo darán lugar a la placenta, por lo que las células que darán origen al feto quedarán intactas, siendo una técnica segura que, en manos expertas, no afecta negativamente al desarrollo normal del embrión.
Cuando los embriones alcanzan la etapa de blastocisto y tienen una calidad suficiente se procede con la biopsia embrionaria. Una vez biopsiados, los embriones son congelados por vitrificación a la espera del resultado del análisis genético.


Test genético pre-implantacional (PGT-A, PGT-M, PGT-SR)
El test genético preimplantacional (PGT, por sus siglas en inglés) se realiza durante la fecundación in vitro (FIV) y permite la detección y prevención de enfermedades genéticas o cromosómicas en los embriones antes de ser transferidos al útero materno para el inicio de la implantación.
Existen tres tipos de PGT que pueden ser utilizados según sea la indicación: PGT-A, PGT-M y PGT-SR.
- PGT-A: se utiliza para la detección de aneuploidias (cromosomas adicionales o faltantes), analizando la composición cromosómica de los embriones antes de ser transferidos. Esta técnica ha permitido mejorar los resultados e incrementar las probabilidades de embarazo al seleccionar los embriones con carga cromosómica correcta.
- PGT- M: evita la transmisión de alteraciones genéticas hereditarias (cambios que alteran la secuencia de nucleótidos del ADN). Permite detectar la alteración o mutación en un gen en concreto que causa una enfermedad monogénica o mendeliana.
- PGT-SR: detecta la presencia de alteraciones estructurales cromosómicas en embriones (cuando un fragmento de un cromosoma individual se rompe y se reubica de algún modo lo cual puede dar lugar a pérdida de material cromosómico), que pueda causar alguna enfermedad o malformación en la descendencia. Se indica en pacientes con antecedentes de alguna alteración cromosómica estructural.